A
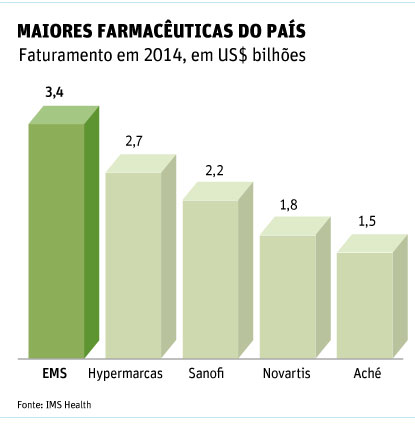
EMS, maior farmacêutica do país em faturamento, está proibida de vender
medicamentos para o poder público.
Também não pode pedir
registro de novas drogas ou renovação das antigas.
A
empresa teve indeferido pela Anvisa (Agência Nacional de Vigilância Sanitária)
pedido de renovação do certificado de boas práticas de fabricação de
medicamentos.
A
decisão foi publicada nesta segunda (2) no "Diário Oficial da União".
O
documento é a garantia de que a empresa tem condições técnicas e operacionais
para a fabricação de remédios. Sem ele, fica com as atividade limitadas.
A medida foi tomada quase um
mês após a Anvisa interditar parte da fábrica da EMS e suspender a fabricação
de dois antibióticos genéricos: a amoxicilina + clavulanato de potássio 50
mg/ml + 12 mg/ml pó para suspensão oral e rifamicina 10 mg/ml, solução tópica
spray.
Conforme
revelado pela Folha, a temperatura do almoxarifado da fábrica em Hortolândia
(SP) estava em 46°C, quando a determinada pelas normas é entre 15°C e 28°C.
Essa condição pode degradar o produto.
No
caso da amoxilina, segundo a Anvisa, a empresa estava utilizando uma substância
não aprovada e sintetizando outra de forma diferente da que foi informada à
agência. Isso pode tornar o remédio ineficaz e com potenciais riscos à
população.
Em
relação à rifamicina, a Anvisa constatou que o laboratório aumentou o tamanho
do lote em dez vezes sem que houvesse aprovação prévia.
CERTIFICADO
Sem
o certificado de boas práticas, a EMS não pode participar de licitações, mas
isso não a impede de vender remédios para as farmácias.
"É
uma idiossincracia, mas amparada pela legislação. Não pode vender para o SUS,
mas pode comercializar para o público", diz Dirceu Raposo de Mello,
professor de farmácia da Anhembi Morumbi e ex-presidente da Anvisa.
Procurada,
a Anvisa informou que não poderia se manifestar sobre a decisão.
Mello
explica que, se a empresa recorrer da decisão, a medida tem efeito suspensivo
até o julgamento do recurso. Em algumas situações, isso pode levar até dois anos.
Outras
duas farmacêuticas pertencentes à EMS, Germed e Legrand, também de Hortolândia,
tiveram negados pedidos de certificados de boas práticas, mas a Anvisa não
informou o motivo. A EMS diz que já tomou providências para resolver o
problema.
Figuram
ainda na lista publicada no "Diário Oficial" o Laboratório
Farmacêutico do Estado de Pernambuco (Lafepe) e a Hypermarcas.
Segundo
diretor-presidente do Lafepe, José Fernando Uchôa, o problema será corrigido em
até 120 dias. Já a Hypermarcas informou que a fábrica que consta na lista está
fechada desde 2011.
OUTRO LADO
A
EMS informou, por nota, que "todas as providências já foram tomadas com a
finalidade de obter a renovação das certificações". A empresa afirma ainda
que o mesmo vale para as outras unidades do grupo, Germed e Legrand.
Segundo
diretor-presidente do Lafepe, José Fernando Uchôa, o pedido de renovação foi
indeferido porque a vigilância encontrou problemas na unidade de pomadas.
"São coisas básicas. Uma parede que não está pintada de forma adequada,
por exemplo."
Ele
diz que a empresa já está corrigindo as irregularidade e solicitará nova
vistoria. "Em até 120 dias esperamos já estar tudo resolvido."
A
Hypermarcas informou que o pedido indeferido se referia a uma fábrica
desativada em 2011. "A produção foi migrada para subsidiária da companhia
em Anápolis, Goiás, que possui os certificados necessários para a fabricação de
medicamentos."
Grifo nosso
Fonte: folhauol.com.br /
Cláudia Collucci
Imagem: Reprodução / folhapress
Curta e compartilhe no
Facebook
Sem comentários:
Enviar um comentário